Genetisch bedingte Fehlbildungen in den Blutgefäßen des Gehirns sind selten, tragen aber eine große Gefahr in sich. Daher suchen Forschende nach einem Medikament, das diese Fehlbildungen verhindert. Einen vielversprechenden Kandidaten haben sie gefunden.
Die familiäre zerebrale kavernöse Malformation (cerebral cavernous malformations, kurz CCM) ist eine seltene genetische Erkrankung, die zu Verwachsungen der Blutgefäße im Gehirn führt. Für die Betroffenen können diese Fehlbildungen lebensgefährlich werden, weil sie Hirnblutungen und Schlaganfälle verursachen können. Wesentlich häufiger als diese seltene erbliche Form der Erkrankung sind spontane CCM-Fehlbildungen, deren Ursachen bislang unklar sind. Unter ihnen leiden Schätzungen zufolge bis zu 400.000 Menschen alleine in Deutschland. „Bislang gibt es für keine der beiden CCM-Formen wirkungsvolle Medikamente.
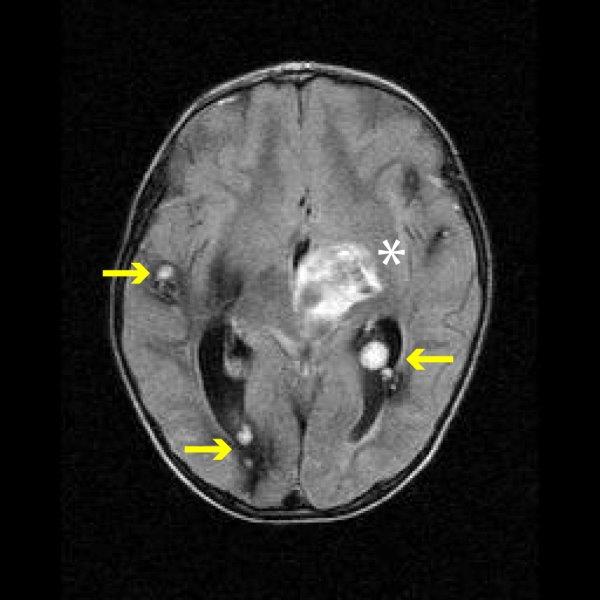
MRT-Aufnahme des Gehirns eines dreijährigen Kindes mit familiärer CCM. Die gelben Pfeile zeigen auf CCM-Läsionen. Der weiße Stern markiert ein Hämatom.
Die einzige Behandlungsmöglichkeit ist, die Fehlbildungen operativ zu entfernen. Das geht allerdings nur, wenn diese nicht zu tief im Inneren des Gehirns oder in überlebenswichtigen Regionen liegen. Wir brauchen daher dringend ein Medikament für die Behandlung der CCM“, sagt Dr. Samil Seyfried, Professor an der Universität Potsdam sowie der Medizinischen Hochschule Hannover. Gemeinsam mit Kolleginnen und Kollegen aus Deutschland, Kanada und Frankreich machte sich der Wissenschaftler auf die Suche nach einem geeigneten Wirkstoff – und wurde fündig: Indirubin-3-Monoxime ist ein Bestandteil des roten Farbstoffs Indigo, der unter anderem in der Leukämie-Therapie eingesetzt wird. Seyfrieds Arbeitsgruppe fand heraus, dass der Wirkstoff im Tiermodell Gefäßverwachsungen verhindert.
Ihre Suche haben die Forschenden auf Wirkstoffe beschränkt, die bereits zur Behandlung anderer Erkrankungen zugelassen waren. Das hat den großen Vorteil, dass sie Indirubin-3-Monoxime bereits im nächsten Schritt in einer klinischen Studie bei Patientinnen und Patienten einsetzen können. Denn wichtige Nachweise – beispielsweise zur Sicherheit und zur Dosierung des Wirkstoffs – sind bereits im Vorfeld der ersten Zulassung erbracht worden.
Wirkstoffbibliothek mit mehr als 5.000 Substanzen
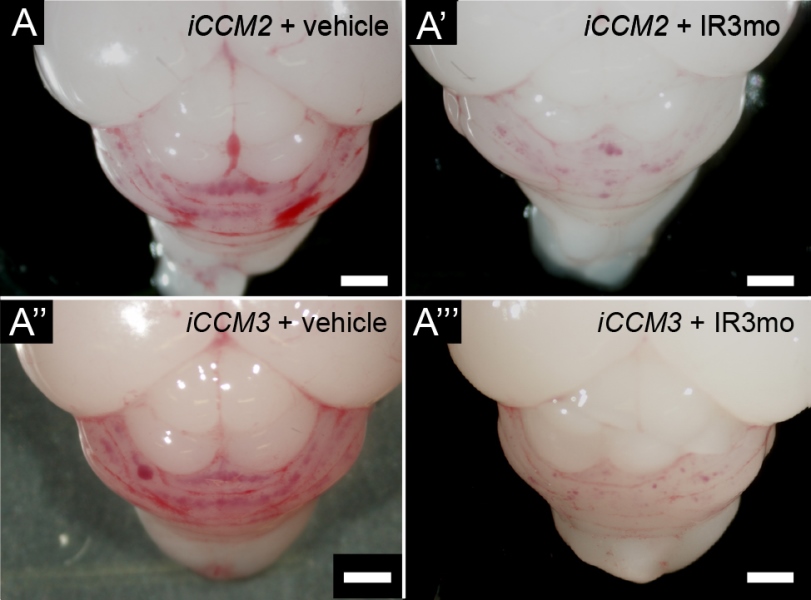
Bilder von der Behandlung zweier unterschiedlicher Mausmodelle mit Indirubin-3-Monoxime. Auf der linken Seite sind unbehandelte Tiere, rechts die behandelten Mausstämme zu sehen.
Insgesamt haben die Wissenschaftlerinnen und Wissenschaftler mehr als 5.000 Substanzen getestet. Um eine derart umfassende Suche durchführen zu können, mussten sie zunächst eine zentrale Datenbank schaffen, die alle Wirkstoffbibliotheken der beteiligten Institutionen zusammenfasst. Im nächsten Schritt testeten die Forschenden des von der Europäischen Union geförderten Konsortiums alle identifizierten Arzneistoffe an Tiermodellen wie Fadenwürmern und Zebrafischeiern, die CCM-ähnliche Symptome ausprägten. Die erfolgreichsten Kandidaten, etwa 130 verschiedenen Wirkstoffe, wurden anschließend in menschlichen Zellen der Blutgefäßwand überprüft. So konnte schließlich die Substanz Indirubin-3-Monoxime identifiziert werden, deren Wirkung auf die Gefäße letztlich in Labormäusen verifiziert wurde. „Wir haben unterschiedliche Krankheitsmodelle eingesetzt, um möglichst viele Aspekte rund um die Entstehung und den Verlauf einer CCM abzudecken. Die einzelnen Modelle ergänzen sich sehr gut – und jedes spielt eine wichtige Rolle für die Wirkstoffsuche“, erläutert Seyfried.
Neue Erkenntnisse über die Entstehung und den Verlauf der CCM
Die umfassenden Informationen, die die Forschenden durch ihre Wirkstoffsuche gewonnen haben, lassen sich aber auch anderweitig nutzen: Sie können wichtige Informationen über die molekularen Hintergründe der CCM liefern. Mithilfe komplexer Software-Analysen konnten die Wissenschaftlerinnen und Wissenschaftler neue Erkenntnisse darüber erlangen, wie die Erkrankungen entstehen und verlaufen. Sie identifizierten bei ihrer Testung beispielsweise Proteine, die an der Entstehung von Gefäßmissbildungen beteiligt sind. Zukünftig könnten diese Proteine Ansatzstellen für neue Therapiemöglichkeiten darstellen – auch für andere Blutgefäßerkrankungen, beispielsweise für den hämorrhagischen Schlaganfall, der durch den Riss eines Blutgefäßes im Gehirn entsteht.
Seltene Erkrankungen „E-Rare“
Bereits seit 2006 beteiligt sich das Bundesministerium für Bildung und Forschung (BMBF) an der internationalen Forschungsinitiative zu seltenen Erkrankungen „E-Rare“, in der auch das hier vorgestellte CCMCURE-Konsortium gefördert wird. Insgesamt 23 Forschungsförderer aus 17 Ländern arbeiten in dieser Initiative eng zusammen. Zum CCMCURE-Konsortium gehören neben der Medizinischen Hochschule Hannover und der Universität Potsdam auch das Hospital for Sick Children (SickKids) in Toronto, die Université Paris Diderot, das INSERM Grenoble sowie das Leibniz-Institut für molekulare Pharmakologie in Berlin.
Ansprechpartner:
Prof. Dr. Salim Seyfried
Medizinische Hochschule Hannover
Institut für Molekularbiologie
Carl-Neuberg-Straße 1
30625 Hannover
0511 532-5933
Universität Potsdam
Institut für Biochemie und Biologie
Karl-Liebknecht-Straße 24−25
14476 Potsdam
0331 977-5540
Salim.Seyfried@uni-potsdam.de