Indem Sie zulassen, dass wir Ihre Besuche auf dieser Webseite anonymisiert mitzählen, helfen Sie uns das Angebot für Nutzerinnen und Nutzer zu optimieren. Dafür verwenden wir Cookies. Die erfassten Daten werden nicht an Dritte weitergegeben. Mehr Informationen finden Sie in unserer Datenschutzerklärung. Wer unsere Dienstleister sind, können Sie im Impressum unter folgendem Link nachlesen: Impressum.
Die hereditäre spastische Spinalparalyse ist eine seltene erbliche Erkrankung. Sie führt zu einer langsam fortschreitenden Spastik und Lähmung der Beine. Erstmals hat ein Forschungsteam eine Therapiemöglichkeit entdeckt und in einer klinischen Studie erprobt.

Meist bricht die SPG5 im Jugendalter aus. Die Betroffenen können oftmals 20 bis 30 Jahre später nicht mehr gehen und sind im Alltag auf einen Rollstuhl angewiesen.
Adam Wasilewski/AdobeStock
Ist die Einnahme des cholesterinsenkenden Medikaments Atorvastatin eine Therapieoption für Patientinnen und Patienten mit hereditärer spastischer Spinalparalyse Typ SPG5? Die Antwort lautet: möglicherweise. Diesen Hinweis gibt eine erste klinische Studie mit Betroffenen, die an dieser seltenen erblichen Nervenerkrankung leiden.
Bei Patientinnen und Patienten mit SPG5 kommt es zu einem schleichenden Funktionsverlust der motorischen Leitungsbahnen im Rückenmark. Ursache hierfür ist ein Defekt im Gen CYP7B1, das am Abbau von Cholesterin zu Gallensäuren beteiligt ist. Fällt CYP7B1 aus, häufen sich im Blut und im Nervenwasser der Patientinnen und Patienten Abbauprodukte von Cholesterin an. Diese Abbauprodukte nennt man Oxysterole. „Wir vermuten, dass die Ansammlung von Oxysterolen nicht nur eine Begleiterscheinung der Erkrankung ist. Vielmehr sind wir der Überzeugung, dass die hohe Konzentration an Oxysterol möglicherweise die Ursache der Erkrankung sein könnte“, sagt Privatdozentin Dr. Rebecca Schüle, Neurologin an der Universitätsklinik Tübingen. Deshalb kam ihr Team gemeinsam mit ihrem Kollegen Professor Ludger Schöls auf die Idee, zunächst zu untersuchen, ob Oxysterole in Konzentrationen, wie sie bei SPG5-Patienten vorliegen, tatsächlich giftig für Nervenzellen sind. Und falls ja, ob der krankhaft erhöhte Oxysterolspiegel bei SPG5-Patienten möglicherweise durch eine cholesterinsenkende Therapie beeinflusst werden kann.
Zur Beantwortung der Frage, ob Oxysterole gefährlich für Nervenzellen sind, haben die Forschenden zunächst ein Modell für humane Nervenzellen generiert: Aus Haut eines gesunden Spenders wurden Bindegewebszellen isoliert. Diese Zellen wurden durch ein Verfahren – genannt Reprogrammierung – in Stammzellen zurückverwandelt. „Stammzellen haben die Fähigkeit, sich in jedes Gewebe des Körpers zu verwandeln. Sie benötigen dazu aber spezifische Signale, die bestimmen, ob sich eine Stammzelle beispielsweise in eine Herzmuskelzelle, eine Leberzelle oder eine Nervenzelle verwandelt“, erklärt Schüle. „Wir haben aus den Stammzellen kortikale Neurone, also die Nervenzellen, gezüchtet, die bei der SPG5 schwerpunktmäßig von der Erkrankung betroffen sind.“
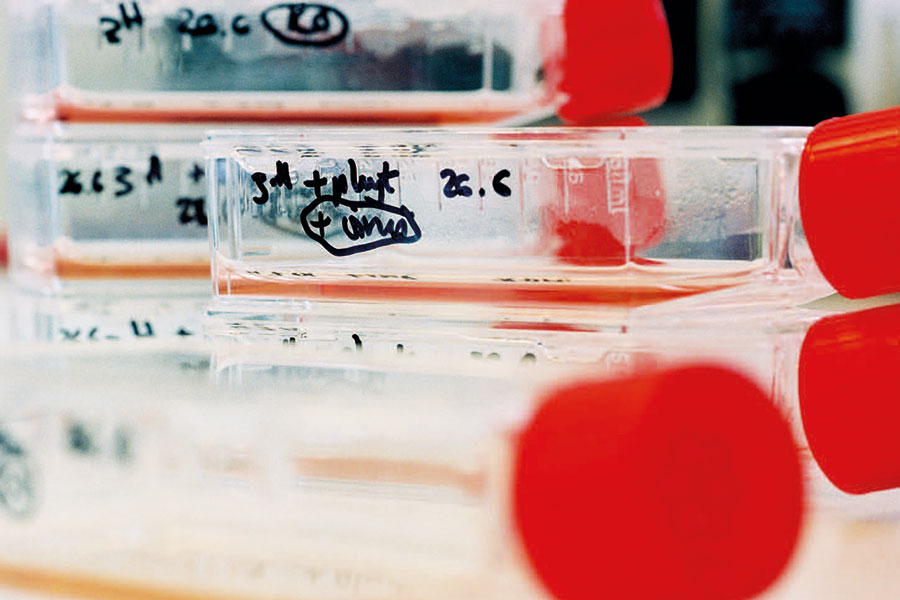
In Versuchen mit Nervenzellen zeigte sich, dass Oxysterole den Stoffwechsel beeinträchtigen
und sogar zum Tod der Zellen führen.
NGFN/BMBF
Die Nervenzellen wurden mit steigenden Konzentrationen von Oxysterolen behandelt und anschließend der Stoffwechsel und die Überlebensfähigkeit der Zellen untersucht. Tatsächlich zeigte sich, dass Oxysterole toxisch für Nervenzellen sind. Während ein niedriger Oxysterolspiegel noch problemlos von den menschlichen Nervenzellen toleriert wird, führen Konzentrationen, wie sie bei SPG5-Patienten vorliegen, zu einer dramatischen Beeinträchtigung der Stoffwechselaktivität der Nervenzellen und sogar zum Tod der Zellen. Das Fazit der Wissenschaftler: Ein erhöhter Oxysterolspiegel kann also direkt für die Funktionsbeeinträchtigung der motorischen Nervenzellen bei der SPG5 verantwortlich sein. Denn im Blut von SPG5-Patienten liegt die Konzentration des Oxysterols 27-Hydroxycholesterol etwa 6-fach höher als bei Gesunden. Im Nervenwasser ist die Konzentration sogar 25-fach erhöht. Die Oxysterolspiegel korrelieren dabei direkt mit der Schwere der Erkrankung: Schwerer betroffene SPG5-Patienten haben höhere 27-Hydroxycholesterolspiegel als wenig betroffene.
Die hereditäre spastische Spinalparalyse Typ SPG5 ist eine sehr seltene erbliche Erkrankung. Derzeit sind weltweit 56 Familien bekannt, die von der Erkrankung betroffen sind. Damit ergibt sich eine geschätzte Häufigkeit von 1 zu 1 Million. SPG5 führt zu einer langsam fortschreitenden Spastik und Lähmung der Beine. Meist beginnt die Erkrankung im Jugendalter und führt im Verlauf zu einer zunehmenden Beeinträchtigung beim Gehen. Betroffene verlieren oftmals 20 bis 30 Jahre nach Ausbruch der Erkrankung ihre Gehfähigkeit und sind im Alltag auf einen Rollstuhl angewiesen. Ursache der Erkrankung ist ein Gendefekt, der zu einem schleichenden Funktionsverlust der motorischen Leitungsbahnen im Rückenmark führt. Der genaue Mechanismus dieses Funktionsverlustes ist unklar, und so stehen bislang auch keine Therapieoptionen zur Verfügung, um den Erkrankungsverlauf zu beeinflussen und die Verschlechterung der Gehfähigkeit aufzuhalten. Betroffene sind derzeit auf rein symptomatische Therapien, wie Krankengymnastik sowie spastiklösende Medikamente und Schmerzmittel, angewiesen.
„Unsere Ergebnisse stimmten uns zuversichtlich, dass eine cholesterinsenkende Therapie tatsächlich ein therapeutischer Ansatz bei SPG5 sein könnte“, erklärt Schüle. Deshalb testeten die Forscherinnen und Forscher die Wirksamkeit des cholesterinsenkenden Medikaments Atorvastatin in einer randomisierten, placebokontrollierten klinischen Studie. Hierzu wurden 14 Patientinnen und Patienten mit SPG5 untersucht. Die Hälfte der Patienten wurde mit Atorvastatin und die andere Hälfte mit einem Placebomedikament behandelt. Die Zuteilung in die Gruppen erfolgte zufällig. Weder die Studienärzte noch die Patienten waren über die Gruppenzuordnung informiert. Zu Beginn der Studie und nach neunwöchiger Therapie wurden Blut und Nervenwasser abgenommen und die Oxysterolspiegel bestimmt sowie die Patienten klinisch untersucht. Das Ergebnis: Die Therapie mit Atorvastatin führte zu einem Rückgang der Oxysterolspiegel im Blut der SPG5-Patienten um rund 30 Prozent. Alle Patienten haben das Medikament gut vertragen. Es gab keine Anzeichen schwerer Nebenwirkungen.
Das Gebiet der seltenen Erkrankungen ist eines der Forschungsfelder, die von einer koordinierten internationalen Zusammenarbeit besonders profitieren können. Das liegt sowohl an der jeweils kleinen Zahl von betroffenen Patientinnen und Patienten als auch an der national unterschiedlich ausgeprägten Forschungsexpertise für die einzelnen Erkrankungen. Daher beteiligt sich das BMBF seit 2006 an der ERA-Net-Initiative „E-Rare“. Derzeit beteiligen sich 23 Forschungsförderer aus 17 Ländern an der Initiative. Eines der in E-Rare geförderten Forschungsnetzwerke ist das beschriebene Projekt.
Mehr Informationen: www.gesundheitsforschung-bmbf.de/de/e-rare-4468.php
„Das sind sehr vielversprechende Ergebnisse“, so Schüle. Zwar ließ sich im Nervenwasser noch kein Einfluss auf die Oxysterolkonzentration nachweisen. Auch gab es bislang keine Veränderung in den klinischen Beschwerden der Studienteilnehmenden. „Eine Verbesserung der Symptomatik hatten wir bei der kurzen Studiendauer auch nicht erwartet“, sagt Schüle. Die Wissenschaftler sind zuversichtlich, dass sie auf dem richtigen Weg sind: „Wir passen derzeit das Therapieregime an, um eine noch stärkere Senkung der Oxysterolspiegel zu erreichen. Außerdem untersuchen wir, wie auch der Spiegel von Oxysterolen im Nervensystem gesenkt werden kann“, beschreibt die Neurologin. „Wir hoffen, dass wir hiermit in Zukunft tatsächlich die erste kausale Therapie für Menschen mit Hereditärer Spastischer Spinalparalyse Typ SPG5 etablieren können.“ Im weiteren Verlauf plant das Forschungsteam eine länger dauernde Studie von etwa zwei Jahren, in der auch Effekte auf die Symptome der Patienten gemessen werden sollen. Rebecca Schüle ist an einem europaweiten Projekt zur Erforschung der SPG5 beteiligt, das vom Bundesforschungsministerium im Rahmen der ERA-Net-Initiative E-Rare unterstützt wird.
Ansprechpartnerin:
Privatdozentin Dr. Rebecca Schüle
Universitätsklinikum Tübingen
Hoppe-Seyler-Straße 3
72076 Tübingen
07071 29-82057
Rebecca.Schuele-Freyer@uni-tuebingen.de