Die erste Idee für ein neuartiges Medikament gegen Vorhofflimmern hatte das Forschungsteam aus Berlin bereits vor über zehn Jahren. Bei der Ausgründung und den ersten klinischen Studien unterstützten sie das BMBF und private Investoren.
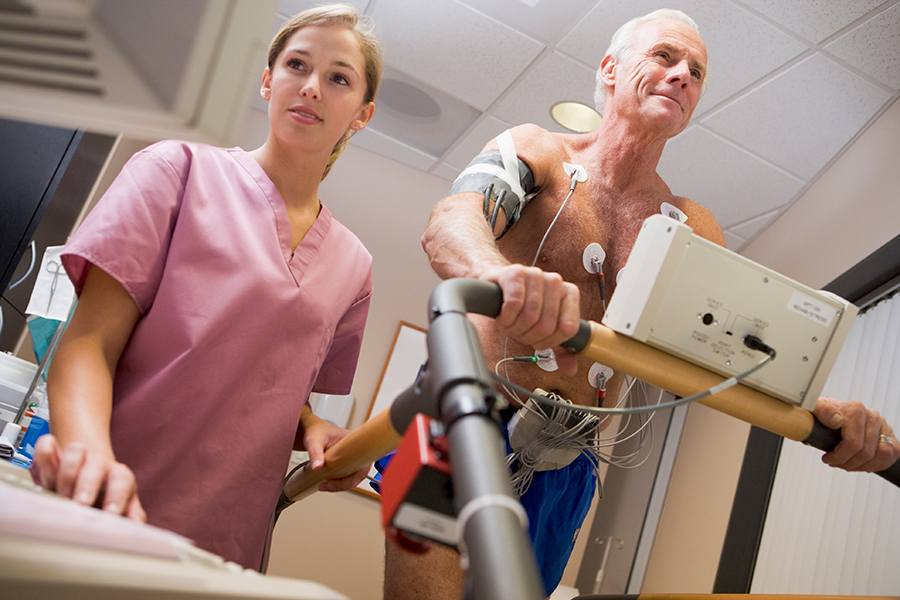
Allein in Deutschland leiden rund zwei Millionen Menschen unter Herzrhythmusstörungen.
monkeybusinessimages/Thinkstock
Der medizinische Fortschritt der vergangenen Jahrzehnte beruht ganz wesentlich auf der Entwicklung neuer Wirkstoffe. Die Forschung stützt sich dabei schon lange nicht mehr auf Zufallsfunde, sondern verfolgt zielgerichtet Angriffspunkte im Körper und testet immer neue Substanzen auf ihre Verträglichkeit und Wirksamkeit. Dennoch bleibt der Weg von der Grundlagenforschung bis zur Anwendung dabei sehr lang und aufwendig. Bevor Wirkstoffkandidaten eine Zulassung als Medikament erhalten, sind umfangreiche und teure Sicherheitsprüfungen notwendig, die ein Großteil nicht besteht. Die Firmen müssen also viel Geld investieren, bevor sie wissen, ob sie mit dem Produkt jemals Geld verdienen. Ein Prototyp für eine neue Maschine lässt sich deutlich schneller bauen und auf den Markt bringen. „Auf dem Weg zum fertigen Medikament muss man Herausforderungen bewältigen. Es ist die teuerste Produktentwicklung mit dem höchsten Risiko“, erklärt Dr. Karen Uhlmann, Mitgründerin von OMEICOS. Das Unternehmen ist eine Ausgründung (Spin-off) aus dem Max-Delbrück-Centrum für Molekulare Medizin (MDC) in Berlin. Im Fokus der Produktentwicklung steht ein neuartiges Medikament gegen Vorhofflimmern – die häufigste Form von Herzrhythmusstörungen. Allein in Deutschland leiden rund zwei Millionen Menschen darunter. Ohne Therapie kann es dabei zu schwerwiegenden Folgen wie einem Schlaganfall kommen.
Vor der Produktidee standen viele Jahre Grundlagenforschung. Die Arbeitsgruppe von Dr. Wolf-Hagen Schunck hat in Zusammenarbeit mit Dr. Robert Fischer und Professor Dr. Dominik Müller am MDC die Wirkmechanismen von Omega-3-Fettsäuren untersucht, die zum Beispiel im marinen Fischöl enthalten sind. Sie konnte zeigen, dass nicht die Fettsäuren selbst potenziell herzschützend sind, sondern spezielle Metabolite, die der Körper als Zwischenprodukte des Stoffwechsels aus diesen Fettsäuren gewinnt. Allerdings sah das Forschungsteam auch, dass diese Metabolite schnell vom Körper weiter verstoffwechselt werden und nur kurzzeitig ihre potenziell guten Eigenschaften entfalten können. Das Forschungsteam hatte früh die Idee, optimierte künstlich erzeugte Kopien – also synthetische Analoga – herzustellen, welche die gleiche oder gar eine bessere Wirkung haben und dabei gleichzeitig stabiler im Körper sind und somit länger ihre Wirkung entfalten können. Inzwischen wird einer der Wirkstoffe an Patientinnen und Patienten getestet.
Für solche Erfolge sind – neben exzellenten wissenschaftlichen Grundlagen – vor allem ein langer Atem und eine zielgerichtete Unterstützung durch öffentliche und private Geldgeber notwendig. Eine Forschungsförderung wie sie in der Grundlagenforschung üblich ist, reicht für die kostenintensive Wirkstoffentwicklung nicht aus. Das Bundesministerium für Bildung und Forschung (BMBF) unterstützt daher gründungswillige Forschungsteams in den Lebenswissenschaften mit speziellen Förderprogrammen, die vielversprechende Projekte in den entscheidenden Phasen begleiten und in vielen Fällen die Akquirierung von privatem Kapital überhaupt erst möglich machen.
Die benötigten Summen sind in der Regel so groß, dass gleich mehrere Risikokapitalgeber, sogenannte Venture Capitalists (VC), Geld investieren müssen. Im Fall von OMEICOS haben öffentliche und private Geldgeber bis heute rund 37 Millionen Euro investiert, wobei auf der Einnahmenseite bislang noch nicht ein Euro umgesetzt wurde. Bis zur Zulassung wird das junge Unternehmen ein Vielfaches brauchen. Im Folgenden zeigen wir anhand einer chronologischen Darstellung der OMEICOS-Ausgründung die Komplexität einer Gründung im lebenswissenschaftlichen Bereich und den anspruchsvollen Weg eines erfolgreichen Transfers.
Vorbereitungsphase (2009−2013)
Ausgründungspotenzial früh erkennen
Ausgangspunkt der Wirkstoffentwicklung waren zunächst theoretische Überlegungen zum Zusammenhang der molekularen Struktur und ihrer biologischen Wirkung. Basierend auf diesen Ergebnissen haben die Forscherinnen und Forscher optimierte Kopien am Reißbrett entworfen, sogenannte synthetische Analoga. Die Analoga sollten eine höhere Stabilität und eine bessere Wirkung als die körpereigene Substanz erzielen. Bei einer Testung in Zelllinien im Labor konnte das Forschungsteam dann erstmals zeigen, dass die künstlichen Analoga die Effektivität der natürlichen Stoffwechselprodukte tatsächlich übertreffen und sich damit für eine mögliche Wirkstoffentwicklung eignen.
Aufgrund des vielversprechenden Potenzials der Analoga stand die Arbeitsgruppe von Schunck schon frühzeitig in engem Austausch mit der Technologietransfer-Abteilung des MDC und hat sich 2009 auf ein sogenanntes PreGoBio-Projekt beworben. Mit dem Programm PreGoBio ermöglicht das MDC eine interne Weiterentwicklung anwendungsbezogener Forschungsvorhaben. Für einen Zeitraum von bis zu drei Jahren erhalten die Projekte zusätzliche Gelder und Beratungsangebote. Außerdem unterstützte sie das Technologietransfer-Unternehmen Ascenion. Die hundertprozentige Tochter der Life-Science-Stiftung deutscher Forschungszentren ist auf den Technologietransfer akademischer Einrichtungen spezialisiert. Sie unterstützt insbesondere Gründungswillige der Leibniz-Gemeinschaft und der Helmholtz-Gemeinschaft, zu der auch das MDC gehört. Die Angebote reichen dabei von Beratungen in Patentfragen bis zu einem individualisierten Coaching bei Ausgründungen.
Durch diese Zusammenarbeit ist auch Uhlmann, damals Mitarbeiterin bei Ascenion, erstmals mit dem Projekt in Berührung gekommen. „Es war früh klar, dass sich das Projekt nicht nur für eine Auslizenzierung eignet, sondern Ausgründungspotenzial hat“, erinnert sich Uhlmann. Die Idee der optimierten Kopien der Stoffwechselprodukte sollte also nicht einfach an eine Pharmafirma verkauft, sondern von einer eigens gegründeten Firma weiterentwickelt werden, da weitere Verwertungsmöglichkeiten erkennbar waren. Bis zur tatsächlichen Ausgründung war es zu diesem Zeitpunkt noch ein weiter Weg. Im Jahr 2009 erzielte das Forschungsteam mit der Einreichung der ersten Patentanmeldung einen ersten wichtigen Meilenstein.
Frühzeitige Unterstützung durch Technologietransfer
Karen Uhlmann
Für einen erfolgreichen Technologietransfer sollten meiner Erfahrung nach die Wissenschaftlerinnen und Wissenschaftler nicht die wirtschaftlichen, patentrechtlichen oder überhaupt die rechtlichen Fragen übernehmen müssen. Hierfür sollten sie die Unterstützung und das umfangreiche Know-how ihrer Transferstellen beanspruchen.
Das Projektteam hat frühzeitig das Potenzial seiner Entdeckung erkannt und die Ausgründung strategisch vorbereitet. Hierzu gehören vor allem die Einbindung wirtschaftlicher, rechtlicher und regulatorischer Expertise und die Vorbereitung einer guten Patentstrategie. Dadurch war das Gründungsteam von OMEICOS bereits in einer frühen Entwicklungsphase gut aufgestellt und kam in die engere Auswahl für ein innovatives Förderinstrument des Bundesministeriums für Bildung und Forschung (BMBF).
Spinnovator-Förderung des BMBF zur Erprobung des Instruments (2011−2014)
Intensive Gründungsvorbereitungen als Schlüssel für eine gelungene Ausgründung
Durch die Zusammenarbeit mit Ascenion stand das Projekt aus der Arbeitsgruppe von Schunck frühzeitig auf der Kandidatenliste für ein neuartiges Förderinstrument des BMBF – den sogenannten Spinnovator. Die Aufnahme in dieses Förderprogramm sollte die Entwicklung des Projekts entscheidend vorantreiben. Neben dem sehr bekannten Förderprogramm Gründungsoffensive Biotechnologie (GO-Bio) hat das BMBF in dieser Zeit einige innovative Instrumente zur Förderung des Transfers im Bereich der Lebenswissenschaften initiiert. Im Spinnovator sollte erprobt werden, ob sich die Erfolgsaussichten der Projekte durch die frühe Einbindung von Technologietransferstellen, Beraterinnen und Beratern sowie Investoren verbessern.
Frühe Einbindung von Investoren
Karen Uhlmann
Insbesondere schon so früh die Investorensicht mit tiefer Branchenkenntnis am Tisch zu haben, war sehr hilfreich. So mussten wir die eigenen Pläne immer wieder einem Realitätscheck unterziehen.

Fischöle sollen das Herz schützen.
rocketclips/Adobe Stock
In einer ersten Phase erhielt zunächst das Technologietransfer-Unternehmen Ascenion eine BMBF-Förderung, um vielversprechende Projekte aus dem eigenen Portfolio auszuwählen und diese bei den Transfervorbereitungen zu unterstützen. Neben einer fundierten Datenlage und einem validen wissenschaftlichen Konzept konnte das OMEICOS-Projekt mit einer guten patentrechtlichen Absicherung überzeugen und kam so auf die Vorschlagsliste. Für die zweite Phase hatten das BMBF und der private Investor Vesalius Biocapital jeweils eine hälftige Unterstützung ausgewählter Forschungsprojekte in Aussicht gestellt, die direkt als Spin-off starten sollten. So hat sich das OMEICOS-Projektteam bereits 2011 zu einem ersten Gespräch mit Vesalius Biocapital und einer Vertretung des BMBF getroffen. „Die frühzeitigen Gespräche mit den Geldgebern haben uns in der kritischen Phase vor der Gründung Selbstvertrauen gegeben“, erinnert sich Uhlmann.
Mit der Aufnahme in das Spinnovator-Programm begann für das Projektteam eine intensive Zeit. Im Zentrum standen dabei der Biochemiker Schunck, der Kardiologe Fischer und die Technologietransfermanagerin Uhlmann. Alle drei sollten später zu den Gründerinnen und Gründern von OMEICOS gehören. Neben der Fortführung der wissenschaftlichen Arbeiten musste das Projektteam innerhalb von knapp zwei Jahren einen Finanz-, Personal- und Businessplan erstellen sowie einen Lizenzvertrag für die Patentrechte und die Eckpunkte für eine Beteiligung der Risikokapitalgeber an der zu gründenden Firma verhandeln. Für den Businessplan gehörte dazu insbesondere eine Abschätzung des Marktpotenzials, eine Analyse möglicher Wettbewerber und eine umfassende Darstellung der Technologie sowie der adressierten Patientenpopulation. „Man muss einen langen Atem haben und dafür ist es sehr wichtig, dass das Team harmoniert. Wenn bei uns einer mal aufgeben wollte, dann wurde er von den anderen mitgezogen“, beschreibt Uhlmann die zwei Jahre vor der Gründung.
Interdisziplinäres Team
Karen Uhlmann
Essenziell für die Gründung war sicherlich das interdisziplinäre und gut harmonierende Team. Nur so konnten wir die verschiedenen Perspektiven vereinen. Dabei war die wissenschaftliche Expertise so wichtig wie die Patientensicht und die umfassenden Kenntnisse im Bereich der wirtschaftlichen und rechtlichen Aspekte.
Bereits während der Gründungsvorbereitungen erkannte das Projektteam, dass das von Vesalius Biocapital und dem BMBF in Aussicht gestellte Geld nicht reichen würde, um alle Pläne für die kommenden fünf Jahre umzusetzen. Das Gründungsteam ging daraufhin auf die Suche nach weiteren Investoren. „Dass wir mit dem BMBF und Vesalius Biocapital bereits zwei finanzstarke und kompetente Partner am Tisch hatten, hat eine Signalwirkung auf andere Investoren gehabt, sich das Projekt genauer anzusehen. Das war ein echter Wettbewerbsvorteil“, erinnert sich Uhlmann.
In dieser Zeit waren allerdings nicht nur unternehmerische Fragen zu klären. Auch im wissenschaftlichen Bereich war ein Wandel notwendig. Aus der Grundlagenforschung musste eine anwendungsorientierte Forschung werden. Eine gute Datenlage zu regulatorischen Aspekten wie etwa der Aufnahme und Ausscheidung des Wirkstoffs im Körper ist für potenzielle Investoren eine Grundvoraussetzung. Parallel dazu musste das Projektteam eine Patentstrategie zur Optimierung der Patentlaufzeit entwickeln. Im Basispatent war zunächst eine Klasse von Molekülen abgesichert. Durch die Anmeldung eines weiteren spezifischeren Patents einige Jahre später konnte der Patentschutz dann für den tatsächlichen Wirkstoff um mehrere Jahre verlängert werden – Jahre, in denen das Unternehmen Geld mit dem Präparat verdienen kann. OMEICOS hat sich damit wiederum attraktiver für mögliche Investoren gemacht.
Mit der Gründung der Firma OMEICOS Therapeutics GmbH im Juni 2013 konnte sich das Team nun voll und ganz auf die Produktentwicklung konzentrieren. Auch die Organisationsstrukturen haben sich damit schlagartig geändert. Die Entscheidungswege in der neu gegründeten Firma waren deutlich kürzer und damit effizienter als zuvor – und nicht zuletzt konnte das Unternehmen endlich Verantwortung für die anstehenden präklinischen und klinischen Studien übernehmen. Nach Abschluss der im Vorfeld gut vorbereiteten Lizenzverträge durfte OMEICOS nun die Substanzen exklusiv nutzen und weiterentwickeln.
Frühzeitige Vernetzung mit Geldgebern
Karen Uhlmann
Die frühzeitige Unterstützung durch das BMBF, die Ascenion und den privaten Investor im Rahmen des Spinnovator-Projekts hat uns in vielerlei Hinsicht bei der Umsetzung unserer Gründungsidee geholfen. Zum einen hatten wir sehr kompetente Partner am Tisch, die uns gut beraten haben. Zum anderen hat die in Aussicht gestellte Summe Türen bei anderen Investoren geöffnet. Dieses Signal darf man nicht unterschätzen.
Durch die Aufnahme im Spinnovator-Programm, die intensive Gründungsbegleitung und die frühe Einbindung des Bundesministeriums für Bildung und Forschung (BMBF) und des Risikokapitalgebers Vesalius Biocapital war OMEICOS bereits bei der Gründung gut aufgestellt. Weitere Schritte in Richtung klinische Studien und Finanzierungsrunden folgten schnell und gut strukturiert.
BMBF-Förderung der hervorgegangenen
Spin-offs (2013−2018)
Signalwirkung für andere Investoren
Nach der Gründung stand endgültig die Umsetzung der Finanzierung durch den Abschluss der Verträge mit den Investoren im Mittelpunkt. Mehrere private Investoren hatten ihr Interesse bekundet und für den Förderantrag beim BMBF fehlte nur noch das förderrechtlich notwendige Eigenkapital der Firma. „Dennoch hat es dann noch eine Weile gedauert, bis der erste Investmentvertrag unterschrieben wurde. Der Frühphaseninvestor Hightech-Gründerfonds (HTGF) hat mit einem Darlehen den Stein ins Rollen gebracht“, so Uhlmann rückblickend. Mit diesem Darlehen konnte die Firma Fördergelder des Pro FIT-Programms der Berliner Investitionsbank gegenfinanzieren, eine wichtige Überbrückungshilfe, um 2014 dann den ersten Finanzierungsvertrag mit privaten Kapitalgebern zu unterzeichnen, der wiederum die BMBF-Fördermittel gegenfinanzierte.
Um das gemeinsame Ziel zu erreichen, den Wirkstoff zügig in die klinische Prüfung zu bringen, musste nach der Gründung ein straffer Zeitplan eingehalten werden. Das BMBF, die privaten Investoren und OMEICOS hatten zu diesem Zeitpunkt eine klare Zeitlinie entlang der regulatorischen Vorgaben im Kopf. Eine Vorbereitungsphase für den Abschluss der präklinischen Arbeiten, dann erste Tests an freiwilligen Probandinnen und Probanden zur Sicherheit des Wirkstoffs und eine dritte Phase zur Überprüfung der Wirksamkeit bei Patientinnen und Patienten mit Vorhofflimmern. Jede Phase endete mit der Erreichung eines Meilensteins, der jeweils eine Wertsteigerung darstellte und damit eine weitere Förderung und weitere Investments ermöglichte. Durch das Spinnovator-Konzept und die Gründungsförderung des BMBF wurde das Projekt dabei konsequent systematisch unterstützt. OMEICOS erhielt so neben der üblichen administrativen und fachlichen Betreuung eine professionelle, unternehmerische Projektbegleitung durch den Projektträger und darüber hinaus die Mittel, um professionelle Beraterinnen und Berater zu finanzieren. Alles zusammen ermöglichte eine stringente und schnelle Weiterentwicklung des
Unternehmens.
Einbindung professioneller Beratung
Karen Uhlmann
Entscheidend für das schnelle Voranschreiten unseres Projekts war die Professionalität auf allen Seiten. Durch die BMBF-Förderung hatten wir unter anderem die Mittel, um externe Beraterinnen und Berater zu finanzieren. Sehr geholfen hat uns auch der Erfahrungsschatz, der über die unternehmerische Begleitung durch den Projektträger in das Projekt geflossen ist. In der Gründungsförderung GO-Bio des BMBF erhalten die gründungswilligen Forschungsteams Seminare zum Beispiel über wirtschaftliche und (patent)-rechtliche Themen. Das ist eine tolle Sache. Bei diesen ‚Gründergesprächen‘ darf ich inzwischen meine Erfahrungen weitergeben.
Mithilfe der ersten Gelder konnte die Firma eigene Labore aufbauen und Personal einstellen. In der zügig vorangetriebenen präklinischen Phase haben die Forscherinnen und Forscher dann die Wirksamkeit und Unbedenklichkeit des Wirkstoffkandidaten OMT-28 in geeigneten Versuchen in Zelllinien und Tiermodellen getestet. OMT-28 ist deutlich stabiler als sein natürliches Pendant und eignet sich mit einer Halbwertszeit von etwa 48 Stunden für einen Einsatz als Medikament. In Laborexperimenten konnte OMEICOS zeigen, dass der Wirkstoff einen körpereigenen Signalweg aktiviert, der den Herzrhythmus stabilisiert und eine schützende Wirkung hat. Damit hatte das Spin-off einen ersten wichtigen Meilenstein erreicht.
Für die Zulassung als Arzneimittel muss ein Wirkstoffkandidat auch noch klinische Studien am Menschen durchlaufen und die strengen Regularien der Arzneimittelzulassungsbehörde erfüllen. Für die klinischen Studien brauchte das junge Unternehmen weitere finanzielle Unterstützung. Die guten Ergebnisse aus der Präklinik konnten die Geldgeber überzeugen. Mit den weiteren eingeworbenen Geldern konnte OMEICOS dann 2017 mit der ersten klinischen Studie zur Prüfung der Verträglichkeit beginnen und das Management verstärken. Auch das BMBF unterstützte das Projekt mit weiteren 1,7 Millionen Euro. In dieser auch Phase I genannten klinischen Studie wird die Sicherheit des Wirkstoffs an gesunden Freiwilligen getestet. „Bisher haben wir großes Glück gehabt. Nicht wenige Wirkstoffkandidaten fallen schon in dieser Phase aufgrund von nicht erwünschten Nebenwirkungen durch“, erläutert Uhlmann.
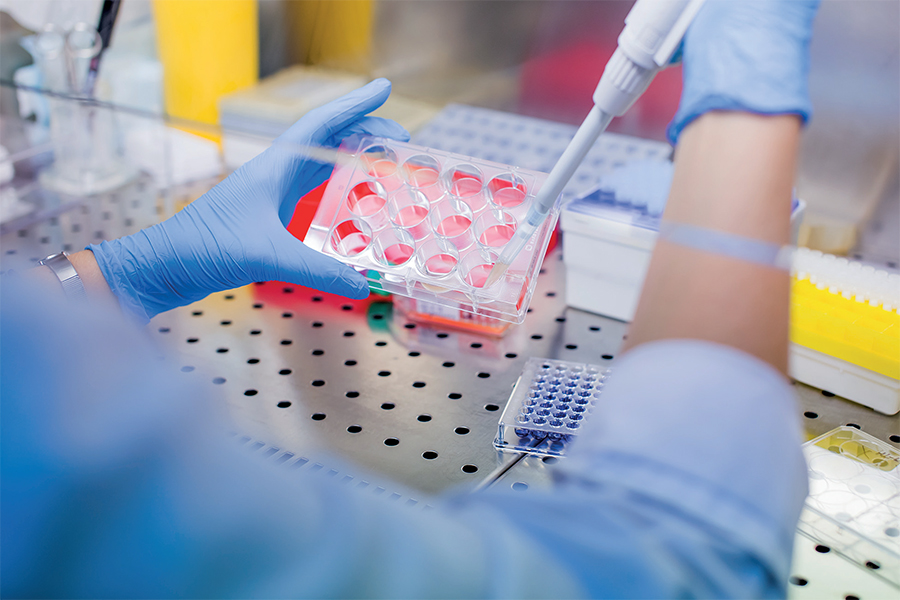
In Laborexperimenten zeigten die synthetischen Analoga eine hohe Stabilität.
Vshyukova/Adobe Stock
Die Firma wuchs nun langsam und nutzte das weitere therapeutische Potenzial der optimierten künstlichen Kopien. So gründete das Unternehmen im Jahr 2017 die Tochterfirma OMEICOS Ophthalmics in den USA, um die Wirksamkeit ihrer Analoga bei Augenerkrankungen zu erforschen. Der Fokus blieb jedoch beim Wirkstoffkandidaten OMT-28 gegen Vorhofflimmern. Nach einem erfolgreichen Abschluss der klinischen Phase I zur Sicherheit des Wirkstoffs hat das Unternehmen den zweiten großen Meilenstein erreicht und kann in einer weiteren Finanzierungsrunde Gelder einwerben, um die klinischen Studien der Phase II vorzubereiten.
„In unserer dritten Finanzierungsrunde 2018 konnten wir mit dem Investor Forbion einen sehr wichtigen großen Fonds überzeugen“, erklärt Frau Uhlmann. So konnte OMEICOS mit der aktuell laufenden Phase II der klinischen Prüfung beginnen, in der erstmals Patientinnen und Patienten mit Vorhofflimmern den Wirkstoff erhalten. In der Studie soll ermittelt werden, wie effektiv OMT-28 den gesunden Herzrhythmus erhalten kann und welches die optimale Dosierung ist, die dann für die nachfolgende Phase III verwendet werden soll. Inzwischen ist die Phase II fast abgeschlossen und noch im Laufe des Jahres 2020 rechnen die Forscherinnen und Forscher mit abschließenden Ergebnissen.
OMEICOS konnte die Finanzierung der nächsten Schritte jeweils sicherstellen. Der Plan war immer, vor der nächsten Finanzierungsrunde einen entscheidenden Meilenstein zu erreichen, der die Geldgeber überzeugt. So konnten gut ausgebildete Mitarbeiterinnen und Mitarbeiter gehalten werden. Wäre die Finanzierung zwischenzeitlich weggebrochen, hätte anschließend neues Personal gesucht und eingearbeitet werden müssen. Das hätte das junge Unternehmen viel Zeit gekostet.
Nach der BMBF-Förderung
Pläne für den Markteintritt
Wenn die Sicherheit und Wirksamkeit bei Patientinnen und Patienten mit Vorhofflimmern in der klinischen Studie Phase II erfolgreich gezeigt werden kann, steht noch eine dritte Phase mit einer großen Gruppe von Betroffenen an. Erst wenn alle drei klinischen Phasen erfolgreich abgeschlossen sind, kann die Zulassung des Medikaments erfolgen. Die Phase III der klinischen Studien kostet ein Vielfaches der vorangegangenen Phasen und kann von kleinen Unternehmen in der Regel auch nicht mehr mithilfe von privaten Investoren gestemmt werden. Wie es für OMEICOS dann weitergeht, ist noch offen. Die teure Phase III können sich in der Regel nur große Pharmafirmen leisten, die mit den kleinen Firmen kooperieren und die Entwicklung des Wirkstoffs übernehmen. „Wir haben bereits viele Kontakte zur Pharmaindustrie aufgebaut. Mit den Firmen müssen wir intensiv sprechen, sobald die Ergebnisse der Phase II vorliegen“, so Uhlmann.
Für die Zukunft hat das kleine Unternehmen bereits weitere vielversprechende Wirkstoffkandidaten für andere Indikationen, etwa aus der Augenheilkunde, im Blick. OMEICOS hofft, dass sich hieraus ein nachhaltiges Geschäftsmodell entwickeln lässt. Bis dahin will die junge Firma aber erst einmal die Entwicklung ihres Wirkstoffs gegen Vorhofflimmern weiterhin schnell vorantreiben, damit er bald bei den Betroffenen ankommt. „Wir rechnen noch mit vier bis fünf Jahren bis zur Zulassung“, sagt Uhlmann. „Vom Beginn der Präklinik bis zur Markteinführung wären das dann rund zehn Jahre – das ist relativ schnell im Vergleich zu anderen Wirkstoffen.“
Im Folgenden sind die einzelnen Transferschritte auf dem Weg von der ersten Idee zu dem Wirkstoff chronologisch gelistet. Wenn Sie auf einen Zeitraum klicken, öffnet sich der dazugehörige Abschnitt.
2009
Die Arbeitsgruppe reicht eine erste Patentanmeldung ein, um ihre grundlegende Erfindung abzusichern. Patente zum Schutz des geistigen Eigentums sind eine wichtige Voraussetzung für eine mögliche Gründung und eine spätere Verwertung der Forschungsergebnisse.
2011
Nach Aufnahme im Spinnovator-Programm finden erste Gespräche mit dem Bundesministerium für Bildung und Forschung (BMBF) und dem privaten Investor Vesalius Biocapital statt. Die Gründung des Spin-offs wird danach zielgerichtet vorangetrieben.
2013
Im Juni wird die Firma OMEICOS Therapeutics GmbH als Spin-off des Max-Delbrück-Centrums ausgegründet. Die Firma kann nun einen Antrag auf eine BMBF-Förderung stellen und weitere private Investoren akquirieren.
2014
Nach einer umfangreichen präklinischen Testung zur Wirksamkeit und Unbedenklichkeit wählt das Spin-off OMT-28 als Wirkstoffkandidaten aus und entwickelt diesen weiter in Richtung klinische Erprobung.
2017
Eine erste klinische Studie an gesunden Freiwilligen (Phase I) zeigt die Sicherheit und Verträglichkeit des Wirkstoffkandidaten. An der randomisierten, doppelblinden, Placebo-kontrollierten Phase I-Studie nahmen 75 Probandinnen und Probanden teil.
2019
Nach einer erfolgreichen Phase I-Studie kann planmäßig eine kombinierte Phase II-Studie zur Effektivität und Dosisfindung mit den ersten Betroffenen starten. In dieser Phase erhält erstmals eine kleine Gruppe von Patientinnen und Patienten mit Vorhofflimmern den Wirkstoffkandidaten.
Ausblick
Die Ergebnisse der klinischen Studien aus Phase II sollen Ende 2020 vorliegen. Das Unternehmen steht bereits in Kontakt mit großen Pharmafirmen, um die aufwendige und teure Phase III der klinischen Studien mit einem Kooperationspartner anzugehen. Bei einem erfolgreichen Abschluss könnte das Medikament den Patientinnen und Patienten bereits 2025 zur Verfügung stehen.