Um die Therapie beim Merkelzellkarzinom zu optimieren, haben Forschende des Deutschen Konsortiums für Translationale Krebsforschung (DKTK) in einer Studie erfolgreich eine adjuvante Behandlung mit einem Immun-Checkpoint-Inhibitor getestet.

Merkelzellen sind Sinneszellen der Haut, die nach ihrem Entdecker, dem Göttinger Medizinprofessor Friedrich Sigmund Merkel, benannt wurden. Sie galten als Ursprungszellen des Merkelzellkarzinoms.
Heute gehen Medizinerinnen und Mediziner allerdings davon aus, dass dieser sehr aggressive Krebs aus Stammzellen der obersten Hautschicht entsteht, die aufgrund von Tumorviren oder einer über einen längeren Zeitraum einwirkenden UV-Strahlung zu Krebszellen entartet sind.
Das Merkelzellkarzinom geht mit einer schlechten Prognose und einer hohen Rückfallquote für die Patientinnen und Patienten einher. Obwohl es zu den seltenen Krebsarten gehört, erkranken in Deutschland jährlich zwischen 800 und 1.000 Menschen daran.
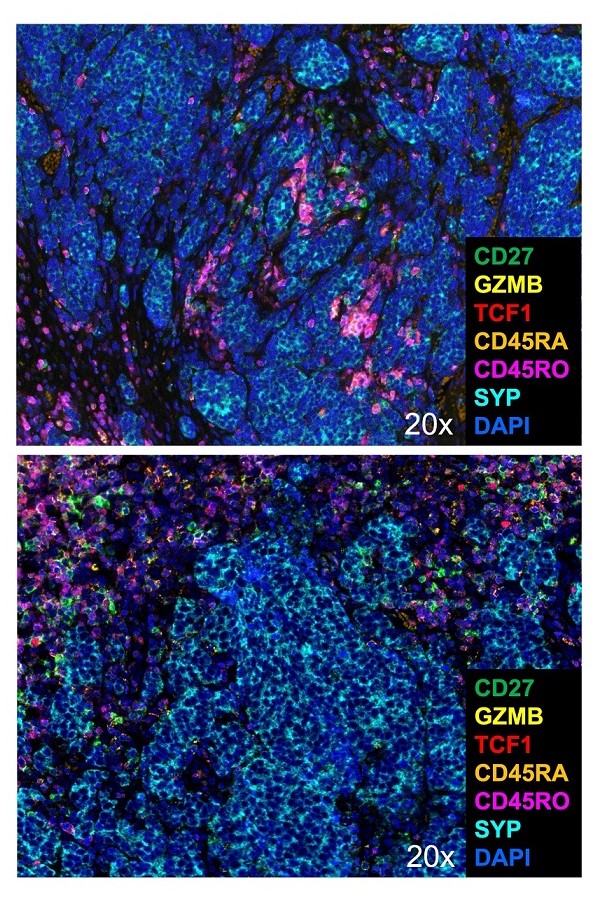
Multiplexe Immunfluoreszenz-Färbungen für T-Zellen und deren Differenzierungsstadien, die ein intratumorales (oben) und ein peritumorales Infiltrat im Merkelzellkarzinom (Syp - Synaptophysin) zeigen. Die oben gezeigte Struktur ist mit einer besseren Prognose verbunden.
Dr. Ivelina Spassova/AG Becker
Studienergebnisse des Deutschen Konsortiums für Translationale Krebsforschung (DKTK) legen nun nahe, dass das Rückfallrisiko dieser Krebserkrankung deutlich sinkt, wenn die Patientinnen und Patienten unmittelbar in Anschluss an die Erstbehandlung – als sogenannte adjuvante Therapie – den Immun-Checkpoint-Inhibitor Nivolumab erhalten. Bislang werden diese Arzneistoffe nur dann eingesetzt, wenn ein Rückfall bereits eingetreten ist oder der Tumor durch eine Operation nicht vollständig entfernt werden konnte.
Die Immunantwort frühzeitig unterstützen
Patientinnen und Patienten mit Merkelzellkarzinom haben häufig bereits zum Zeitpunkt der Diagnose kleinste, mit diagnostischen Untersuchungen nicht erkennbare Metastasen. Dadurch kann der Krebs leicht zurückkehren. Hier greifen Immun-Checkpoint-Inhibitoren wirkungsvoll ein, indem sie die körpereigene Abwehr im Kampf gegen die verbliebenen Krebszellen stärken.
Wird diese Therapie allerdings als adjuvante Behandlung durchgeführt, besteht die Möglichkeit, dass auch die Patientinnen und Patienten behandelt werden, die frei von Tumorzellen sind und eigentlich keiner zusätzlichen Behandlung bedürften. „Daher ist es besonders wichtig, Medikamente einzusetzen, die bereits gut untersucht sind, um mögliche Nachteile und Nebenwirkungen so gering wie möglich zu halten“, erklärt DKTK-Professor Dr. Dr. Jürgen C. Becker, Leiter der Abteilung „Translational Skin Cancer Research“ am Deutschen Krebsforschungszentrum (DKFZ) und am DKTK-Partnerstandort Essen/Düsseldorf an der Universitätsmedizin Essen (UME).
Für ihre multizentrische Studie entschieden sich die DKTK-Forschenden daher für Nivolumab, da der monoklonale Antikörper in der Therapie eine gute Wirkung mit verhältnismäßig geringem Nebenwirkungsspektrum zeigte. „Mögliche Nebenwirkungen gehen, wie bei einer Immuntherapie üblich, mit der gewünschten Wirkung einer gesteigerten Immunantwort einher. Diese kann sich nicht nur gegen den Tumor, sondern auch als Autoimmunreaktion gegen das körpereigene Gewebe richten und zu Entzündungen in verschiedenen Körperregionen führen, meist an der Haut oder im Darm“, erklärt Becker.
Studie zeigt deutlich verringertes Rückfallrisiko
In Essen werden seit Jahren zahlreiche Patientinnen und Patienten mit Merkelzellkarzinom behandelt. Für die Studie war es aber aufgrund der Seltenheit der Erkrankung wichtig, die Rekrutierung auf weitere Standorte und Zentren auszuweiten. Die Studienzentren untersuchten zwischen 2014 und 2020 insgesamt 179 Patientinnen und Patienten mit Merkelzellkarzinom, die auch nach operativer Entfernung ein hohes Risiko für einen Rückfall hatten. Sie erhielten monatliche Dosen von jeweils 480 mg Nivolumab über einen Zeitraum von zwölf Monaten; die Kontrollgruppe wurde entsprechend dem aktuellen Therapiestandard regelmäßig überwacht.
Immun-Checkpoint-Inhibitoren
Immun-Checkpoints sind wichtige Schaltstellen des Körpers zur Steuerung von Immunantworten. Dabei handelt es sich um Zellrezeptoren, die auf der Membran von Immunzellen (T-Zellen) vorkommen und deren Aktivität steuern. Krebszellen können das ausnutzen, indem sie bestimmte Checkpoints und damit die gegen sie gerichtete Abwehr ausschalten. Immun-Checkpoint-Inhibitoren wirken dem entgegen und verstärken die Immunantwort gegen die Tumorzellen. Sie werden bereits bei vielen Krebserkrankungen erfolgreich eingesetzt
„Das relative Risiko, innerhalb der ersten beiden Jahre einen Rückfall der Erkrankung zu erfahren, reduzierte sich um ungefähr 40 Prozent, das ist ein bemerkenswerter Fortschritt für eine so aggressive Hautkrebsvariante“, fasst Becker die Studienergebnisse zusammen. „Insbesondere Patientinnen und Patienten, die jünger als 65 Jahre sind, profitieren unserer Studie zufolge von der adjuvanten Immuntherapie mit Nivolumab.“ Die beobachteten Nebenwirkungen ähneln denen, die bei der Behandlung anderer Tumoren mit Immun-Checkpoint-Inhibitoren auftreten.

Professor Dr. Dr. Jürgen Becker
DKTK/J. Becker
Suche nach prognostischen Biomarkern
„Es gibt jedoch weiteren Forschungsbedarf, bevor konkrete Therapieleitlinien formuliert werden können“, sagt Becker. Zukünftig wollen die Forschenden des DKTK die gewonnenen Daten daher eingehend analysieren. „Wir haben dafür Gewebeproben gesammelt, zudem wurden die Krankheitsverläufe sehr gut dokumentiert. Das gibt uns die Möglichkeit, im Nachgang zu analysieren, welche Patientinnen und Patienten ein hohes Risiko für die Bildung von Metastasen aufweisen und damit besonders von einer adjuvanten Therapie profitieren würden“, sagt Becker über die nächsten Schritte. Sie hoffen prognostische und prädiktive Biomarker zu finden, um diese Hochrisikopatienten und -patientinnen gezielt bestimmen zu können. Neben den Markern könnte zudem in einer Folgestudie eingehender untersucht werden, wie sich beispielsweise eine Änderung des Behandlungsbeginns oder der Behandlungsdauer auswirken würde.
Originalpublikation:
Becker, J. C., Ugurel, S., Leiter, U., et al. (2023). Adjuvant immunotherapy with nivolumab versus observation in completely resected Merkel cell carcinoma (ADMEC-O): disease-free survival results from a randomised, open-label, phase 2 trial. Lancet. 2023;402(10404):798−808. DOI: 10.1016/S0140-6736(23)00769-9
Deutsches Konsortium für Translationale Krebsforschung (DKTK)
Das Deutsche Konsortium für Translationale Krebsforschung (DKTK) ist eine gemeinsame langfristige Initiative des Bundesministeriums für Bildung und Forschung (BMBF), der beteiligten Bundesländer, des Deutschen Krebsforschungszentrums (DKFZ) als Kernzentrum des DKTK sowie onkologisch besonders ausgewiesenen Forschungseinrichtungen und Kliniken in Translationszentren an acht Standorten in Deutschland: Berlin, Dresden, Essen/Düsseldorf, Frankfurt/Mainz, Freiburg, Heidelberg, München und Tübingen. Das Konsortium wurde als eines der Deutschen Zentren der Gesundheitsforschung (DZG) gegründet. Es fördert interdisziplinäre präklinisch-translationale Forschungsthemen, um Ergebnisse möglichst schnell in neue Ansätze zur Prävention, Diagnostik und Behandlung von Krebserkrankungen zu übertragen und Strategien für die personalisierte Onkologie zu entwickeln. Weitere Informationen über das DKTK gibt es unter: www.dktk.org
Ansprechpartner:
Prof. Dr. Dr. Jürgen Becker
Deutsches Konsortium für Translationale Krebsforschung (DKTK)
Deutsches Krebsforschungszentrum
Translational Skin Cancer Research – TSCR
Med. Fakultät der Universität Duisburg-Essen
Universität Duisburg-Essen
Universitätsstraße 2
45141 Essen
E-Mail: j.becker@dkfz.de
Pressekontakt:
Dr. Nadine Ogrissek
Deutsches Konsortium für Translationale Krebsforschung (DKTK)
Deutsches Krebsforschungszentrum (DKFZ)
Stiftung des öffentlichen Rechts
Im Neuenheimer Feld 280
69120 Heidelberg
Tel.: 06221 42-1646
E-Mail: nadine.ogrissek@dkfz.de