Das multiple Myelom ist eine aggressive Form von Blutkrebs. Immuntherapien können die Überlebenschancen der Betroffenen deutlich erhöhen, bergen jedoch die Gefahr starker Nebenwirkungen. Forschende entwickeln ein KI-Tool für die Risikoeinschätzung.
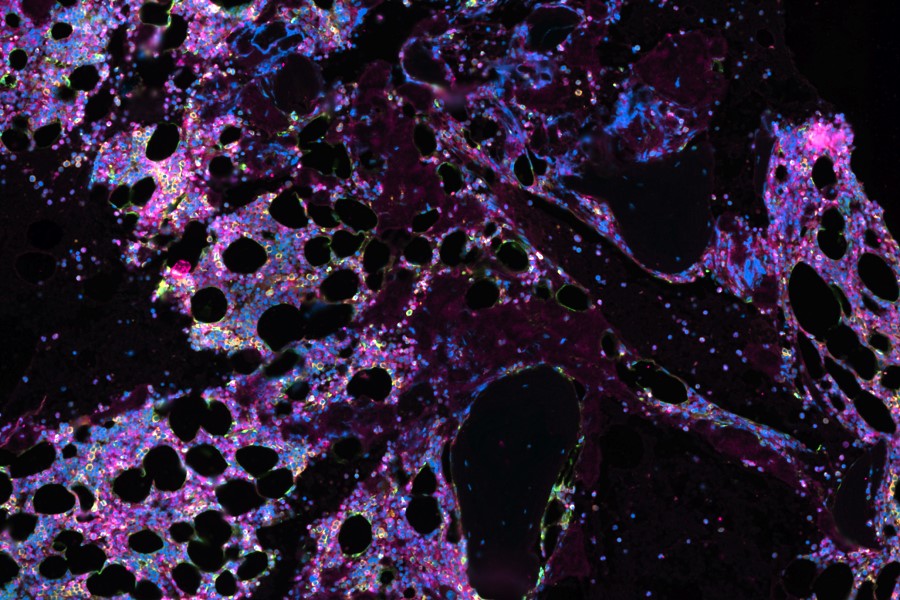
Die Aufnahme zeigt einen Gewebeschnitt des Knochenmarks eines Myelom-Patienten nach der Immuntherapie. Mit Hilfe der KI können die Forschenden räumliche Muster in der Gewebestruktur entschlüsseln und damit Rückschlüsse ziehen, wie sich das Knochenmark im Laufe der Therapie verändert hat.
Arbeitsgruppe Grün
Das multiple Myelom zählt zu den häufigsten Tumorerkrankungen von Knochen und Knochenmark. Hierbei kommt es zu einer unkontrollierten Vermehrung entarteter weißer Blutzellen, die eigentlich für die Immunabwehr zuständig sind. Die bösartigen Tumorzellen breiten sich im Knochenmark aus und stören dort massiv die Blutbildung. Knochenabbau und Nierenversagen sind weitere Folgen der Erkrankung. Das multiple Myelom gilt bisher als unheilbar, die Betroffenen sterben oftmals zwischen fünf und zehn Jahre nach der Diagnose. In den vergangenen Jahren sind die Überlebenschancen durch neue Behandlungsmöglichkeiten jedoch deutlich gestiegen. Besonders vielversprechend sind gezielte Therapien, bei denen das körpereigene Immunsystem gegen die Krebszellen mobilisiert wird.
Doch bislang greifen die Immuntherapien nicht bei allen Patientinnen und Patienten gleichermaßen. Im Gegenteil: Bei einigen Erkrankten lösen sie schwere Nebenwirkungen wie Entzündungen des Knochenmarks und Blutarmut aus, die ebenfalls lebensbedrohlich sein können. Hier setzt das Projekt „TissueNet“ an: „Wir wollen verstehen, warum manche Patienten die Therapien gut vertragen und andere nicht“, sagt Professor Dr. Dominic Grün von der Universität Würzburg. Der Physiker entwickelt gemeinsam mit seinen Kolleginnen und Kollegen eine Künstliche Intelligenz (KI), die künftig vorhersagen könnte, wie bestimmte Patientinnen und Patienten auf die Therapie reagieren werden. Das Bundesministerium für Bildung und Forschung (BMBF) unterstützt das Projekt im Rahmen der Förderinitiative „Computational Life Sciences – CompLS“.
„Mund auf!“ – so lautet das Motto des diesjährigen Weltblutkrebstages. Damit verbindet die Deutsche Knochenmarkspenderdatei (DKMS) als Initiatorin den Appell, sich als Stammzellspenderin oder -spender registrieren zu lassen. Alle zwölf Minuten erhält laut DKMS ein Mensch in Deutschland die Diagnose Blutkrebs. Eine Stammzelltransplantation bedeutet für viele Betroffene deutlich verbesserte Überlebenschancen.
Risikogruppen schon vor der Therapie identifizieren
Die Forschenden wollen herausfinden, was im Knochenmark der Patientinnen und Patienten während der Behandlung genau passiert und welche Schlüsse sich daraus für den weiteren Verlauf der Erkrankung ziehen lassen. Hierfür analysieren sie, wie sich einzelne Zellen im Knochenmark im Laufe einer Immuntherapie genetisch verändern. Dabei nehmen die Wissenschaftlerinnen und Wissenschaftler sowohl die Veränderungen innerhalb als auch im räumlichen Umfeld der Zellen in den Blick. Grundlage der Analyse sind Gewebeproben aus dem Knochenmark von betroffenen Patientinnen und Patienten der Universitätsklinik Würzburg, die jeweils vor und nach der Behandlung entnommen werden. „Das sind riesige Datensätze, die wir untersuchen, zehntausende Daten für jeden einzelnen Patienten und hunderttausende für die erfasste Gruppe insgesamt“, erklärt Grün.
Diese riesige Datenmenge fließt in das Training von KI-Tools ein, mit deren Hilfe die Forschenden rekonstruieren wollen, wie sich die Zellen im Knochenmark der Krebskranken während der Behandlung verändert haben und welche Unterschiede dabei auftreten. „Wir versuchen aus dem Vergleich von Anfangs- und Endzustand so viel Informationen zu ziehen wie möglich, damit die KI möglichst präzise simulieren kann, was in der Zwischenzeit passiert ist“, sagt Grün.
Künftig könnte diese KI Ärztinnen und Ärzte dabei unterstützen, auf Basis einer einzelnen Knochenmarks-Probe eines Erkrankten genau vorherzusagen, ob er zu einer Risikogruppe für schwere Nebenwirkungen gehört. Die Forschenden hoffen zudem, dass sie neue Angriffspunkte für Medikamente identifizieren, die drohende Therapie-Schäden möglichst früh verhindern könnten. Die Methoden seien schon sehr weit ausgereift, so Grün, bis sie jedoch in der klinischen Praxis ankommen, werde es noch eine Weile dauern. Eine Voraussetzung hierfür sei natürlich auch die Bereitschaft der Patientinnen und Patienten, ihre Proben zur Verfügung zu stellen. Grün ist sich sicher: „Mit Hilfe der KI lässt sich die Lebenserwartung und Lebensqualität von Menschen mit multiplem Myelom noch einmal deutlich verbessern.“
Förderung innovativer Softwaretools
In der Patientenversorgung und der klinischen Forschung wächst die Menge an elektronisch verfügbaren Daten rasant. Intelligente Algorithmen können in diesen riesigen Datensätzen versteckte Muster aufspüren. Sie helfen dabei, Zusammenhänge zu erkennen sowie verbesserte Ansätze für die Prävention, Diagnose und Therapie von Krankheiten zu finden. Mit der Förderinitiative „Computational Life Sciences - CompLS“ treibt das Bundesministerium für Bildung und Forschung (BMBF) die Entwicklung innovativer Softwaretools für die Lebenswissenschaften voran. Einer der Schwerpunkte ist die Nutzung von Methoden der Künstlichen Intelligenz in der Biomedizin. Seit 2018 hat das BMBF rund 52 Millionen Euro für mehr als 70 Forschungsprojekte bereitgestellt.