Zahlreiche kleine Veränderungen im Erbgut tragen dazu bei, dass eine Schizophrenie entsteht. Doch welche Veränderungen sind das genau? Und welchen Einfluss üben sie aus? Forschende in Münster suchen nach Antworten auf diese Fragen.
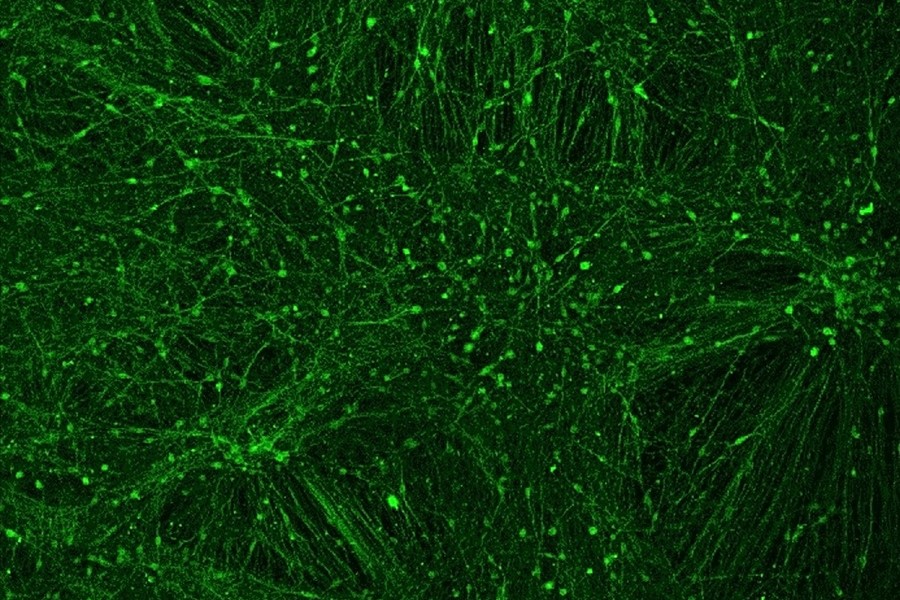
In der Petrischale hergestellte menschliche Neuronen, die in der genannten Studie als Modellsystem zum Studium der genetischen Varianten eingesetzt wurden.
Universität Münster/AG Ziller
Ob ein Mensch an Schizophrenie erkrankt – oder nicht –, wird zu einem großen Anteil auch durch das Erbgut bestimmt. In einem komplexen Zusammenspiel von Genetik und äußeren Einflüssen entsteht eine Erkrankung, die mit einem hohen Leidensdruck einhergeht – für die Betroffenen selbst, aber auch für Angehörige und Freunde.
Rund 50.000 verschiedene genetische Veränderungen wurden in den vergangenen Jahren bei Menschen nachgewiesen, die an Schizophrenie erkrankt sind. Doch nur bei den allerwenigsten dieser Genveränderungen ist bekannt, wie sie wirken. Zudem liegen die meisten von ihnen in Regionen des Erbguts, über die wir bis heute noch nicht viel wissen.
„Unser Ziel ist es, diese Genvarianten zu entschlüsseln. Wir möchten verstehen, welche Varianten wirklich zur Entstehung der Erkrankung beitragen und welche Prozesse im menschlichen Gehirn durch sie gestört werden. Vielleicht finden wir in Zukunft dann eine Möglichkeit, diese Prozesse wieder zu normalisieren – und so wirkungsvolle Therapieansätze gegen Schizophrenie zu entwickeln“, erläutert Professor Dr. Michael Ziller, der an der Universität Münster eine durch das Bundesministerium für Bildung und Forschung (BMBF) geförderte Nachwuchsgruppe in der Systemmedizin geleitet hat.
Schizophrenie
Schizophrenie ist eine Erkrankung des zentralen Nervensystems, unter der weltweit etwa ein Prozent der Menschen leiden. Sie tritt häufig mit Halluzinationen und kognitiven Beeinträchtigungen in Erscheinung und schränkt daher die Lebensqualität der Erkrankten stark ein und belastet auch ihr soziales Umfeld. Eine Heilung der Erkrankung ist bislang nicht möglich, die Symptome können medikamentös aber gelindert werden.
Gemeinsam mit seinen Kolleginnen und Kollegen hat Ziller ein Hochdurchsatzverfahren entwickelt, mit dem er parallel Zehntausende genetische Varianten auf ihre biologischen Funktionen testen kann. Herausgekommen ist dabei eine genetische Landkarte, welche die für Schizophrenie relevanten Varianten und ihre Verbindungen untereinander darstellt.
Nur wenige Genvarianten sind tatsächlich relevant
„Durch unsere Untersuchungen konnten wir nachweisen, dass lediglich 1,7 Prozent der beschriebenen Varianten zur Entstehung einer Schizophrenie beitragen können. Dieser Fakt war bislang unbekannt“, so Ziller. „Welche Auswirkungen diese genetischen Veränderungen in den betroffenen Hirnzellen haben und wie sie sich gegenseitig beeinflussen, wussten wir allerdings zunächst nicht.“

Professor Dr. Michael Ziller gemeinsam mit Dr. Miriam Gagliardi, Erstautorin der Cell-Publikation.
Universität Münster/M. Heine
Im nächsten Schritt identifizierten die Wissenschaftlerinnen und Wissenschaftler dann den Typ von Nervenzellen, in denen die zuvor identifizierten Genvarianten den größten Effekt zeigten, und entwickelten ein entsprechendes Modellsystem. Dadurch war es ihnen möglich, die biologische Funktion der Genvarianten genauer zu untersuchen und ihre Auswirkungen auf die Nervenzellen und neuronalen Netzwerke im menschlichen Gehirn zu verstehen. Die Forschenden wiesen unter anderem nach, dass einige der Genvarianten den Cholesterin- und Fettstoffwechsel in den Zellen beeinflussen und so dazu beitragen, dass die Nervenzellen nur noch eingeschränkt aktiviert werden können. Dieser Effekt könnte zur Entstehung oder zum Verlauf der Erkrankung beitragen.
Das Zusammenspiel unterschiedlicher Faktoren ist entscheidend
Eine wesentliche Voraussetzung für den Erfolg des von Ziller geleiteten Forschungsprojektes war die Expertise aus unterschiedlichen Fachbereichen. So arbeiteten Fachkräfte aus der klinischen Versorgung, der Genetik, der Biologie, der Physik und der Bioinformatik eng im Team zusammen.
Systemmedizin
Ob Herz-Kreislauf-Erkrankungen, Demenz oder Krebs – viele Krankheiten haben eines gemeinsam: Entstehung, Verlauf und Therapieerfolg hängen von zahlreichen Faktoren ab. Dazu gehören die genetische Veranlagung, der persönliche Lebensstil und die äußeren Einflüsse. Das Wissen über die Rolle dieser Faktoren wächst dank der modernen Forschung rasant an. Aufgabe der Systemmedizin ist es, das Zusammenspiel all dieser Faktoren umfassend und mithilfe von mathematischen Modellen zu entschlüsseln – und so den Weg für neue Therapien und Präventionsstrategien zu ebnen. Dafür verzahnt sie neueste Erkenntnisse aus der lebenswissenschaftlichen Grundlagenforschung und der Medizin mit dem Wissen und den Methoden aus Informatik, Mathematik und Physik.
Nun werden die Forschenden auch noch die restlichen von ihnen identifizierten Genvarianten, die sie bislang noch nicht näher untersucht haben, systematisch aufarbeiten. Ihr Blick richtet sich dabei nicht nur auf Auswirkungen der jeweiligen Variante, sondern insbesondere auf ihr Zusammenspiel untereinander. „Denn Schizophrenie entsteht nicht durch eine einzelne genetische Veränderung. Entscheidend ist der gemeinsame Effekt von ganz vielen Varianten. Jede einzelne zeigt kaum eine Wirkung − hinzu kommen äußere Einflüsse, etwa emotionaler oder sozialer Stress“, beschreibt Ziller. Für diese Untersuchungen entwickelt das Forschungsteam neue computergestützte Verfahren, auch um die Patientinnen und Patienten anhand ihrer Variantenkombinationen genauer charakterisieren zu können.
Originalpublikation:
Rummel, C. K., Gagliardi, M., Ahmad, R. et al. (2023). Massively parallel functional dissection of schizophrenia-associated noncoding genetic variants. Cell (2023). 186(23):5165-5182.e33. DOI: 10.1016/j.cell.2023.09.015.
Ansprechpartner:
Prof. Dr. Michael Ziller
Cells in Motion (CiM) Interfaculty Centre
Universität Münster
Röntgenstraße 16
48149 Münster
ziller@uni-muenster.de